Bien que les bêta-amyloïdes aient une grande importance dans la maladie d’Alzheimer et qu’elles participeraient, selon plusieurs, à la survenue de la maladie, de nombreuses questions demeurent. En effet, un grand nombre d’essais cliniques n’ont pas réussi à démontrer que des médicaments conçus pour éliminer les bêta-amyloïdes (ou A bêta) du cerveau pouvaient arrêter ou même seulement ralentir l’évolution de la maladie. Deux équipes de recherche du CCNV ont récemment publié dans Nature Communications des articles qui offrent de nouveaux renseignements sur la façon dont ces A bêta se développent dans le cerveau et mènent au déclin cognitif. Ces deux études nous permettent ainsi d’approfondir nos connaissances au sujet de cette maladie neurodégénérative complexe.
A bêta 34 : une nouvelle pièce dans le casse-tête de la maladie d’Alzheimer
On sait depuis longtemps que les A bêta sont issues du clivage, ou de la coupure, du précurseur de la protéine amyloïde (APP) en structures plus petites. La longueur de ces A bêta varie de 30 à 51 acides aminés. Les plus neurotoxiques sont celles qui comportent 42 acides aminés, appelées « A bêta (Aβ) 42 ». Celles-ci s’agglutinent les unes aux autres pour former des amas collants appelés « plaques amyloïdes » que l’on retrouve dans le cerveau des personnes vivant avec la maladie d’Alzheimer. Une nouvelle découverte dans ce domaine a été réalisée dans le laboratoire du Dr Gerhard Multhaup (professeur et titulaire de chaire, Département de pharmacologie et de thérapeutique) au Complexe des sciences de la vie de l’Université McGill. Dans une récente publication (Aβ34 is a BACE1-derived intermediate associated with amyloid clearance and Alzheimer’s disease progression, Nature Communications, 10:2240), l’équipe du Dr Multhaup présente le lien existant entre un espèce d’A bêta qu’elle a découverte, l’Aβ34, et la maladie d’Alzheimer. L’équipe a découvert que l’Aβ34 est créé lorsque l’Aβ40 et l’Aβ42 sont dissociés en plus petites molécules non toxiques par la bêta sécrétase 1 (BACE1), une enzyme qui participe aussi au clivage de l’APP en Aβ40 et Aβ42 et, donc à la création de plaques amyloïdes dans le cerveau. Donc la BACE1 aurait à la fois des effets négatifs (clivage de l’APP en AB42) et positifs (clivage de l’Aβ42 en Aβ34). Cette découverte suggère que les médicaments qui visent à inhiber l’activité de la BACE1 pourraient en fait nuire, car ils réduiraient aussi les effets bénéfiques de la BACE1. L’équipe du Dr Malthaup décrit également dans cet article que les taux d’Aβ34 sont élevés chez les personnes présentant des troubles cognitifs légers, un stade qui précède souvent la maladie d’Alzheimer, et que les personnes qui ont un taux élevé de Aβ34 ont aussi un débit de clairance de l’Aβ plus élevé. De plus, cette équipe suggère qu’utiliser le rapport Aβ34/Aβ40, au lieu du rapport Aβ40/Aβ42 actuellement utilisé par les cliniciens, pourrait offrir un moyen plus efficace de suivre le développement de la maladie et aider à la diagnostiquer plus rapidement. Ensemble, ces découvertes suggèrent que l’Aβ34 pourrait jouer un rôle important dans le diagnostic précoce de maladie d’Alzheimer et dans le suivi des traitements potentiels futur.
A bêta et déclin cognitif : une relation indirecte
Un des aspects les plus déroutants dans la maladie d’Alzheimer est que les taux d’A bêta (Aβ) dans certaines régions du cerveau ne corrèlent pas bien les dysfonctions cognitives spécifiques des personnes vivant avec la maladie d’Alzheimer. Autrement dit, les régions du cerveau où les taux d’ Aβ s’accumule ne correspondent pas aux régions responsables des fonctions cognitives atteintes. Au Centre de recherche Douglas, l’équipe du Dr Pedro Rosa-Neto (professeur agrégé et directeur, Centre de recherche sur le vieillissement de l’Université McGill) s’est penchée sur cette contradiction apparente dans leur récente publication (Aβ-induced vulnerability propagates via the brain’s default mode network, Nature Communications, 10:2353). L’équipe du Dr Rosa-Neto a déterminé que les Aβ agissent sur le déclin cognitif en un processus à deux étapes. D’abord l’accumulation Aβ dans une région du cerveau rend vulnérable une deuxième région en diminuant le métabolisme de celle-ci. Puis, la présence d’Aβ dans cette deuxième région, combinée à la diminution métabolique conduit au déclin cognitif. Les régions où se déroulent ces processus font toutes parties du réseau cérébral « mode par défaut », un réseau de régions du cerveau qui interagissent entre elles et qui sont associées au repos à l’état d’éveil, à la pensée dirigée envers autrui, à l’autoréflexion, aux souvenirs et à la planification. L’équipe du Dr Rosa-Neto a d’abord démontré ce processus en deux étapes chez les humains puis l’a reproduit dans un modèle animal de la maladie d’Alzheimer. Ceci est d’autant plus intéressant qu’il existe une différence entre le modèle classique de la maladie d’Alzheimer chez l’humain et le modèle animal. Dans le modèle animal, l’accumulation de plaques amyloïdes n’est pas accompagnée d’une accumulation enchevêtrements tau (une autre protéine associée à la maladie), comme c’est le cas chez l’humain. Cela suggère donc qu’il existe un mécanisme de neurodégénérescence indépendant de la protéine tau. Ces résultats indiquent un nouveau rôle des AB dans le déclin cognitif et pourraient représenter une cible permettant de retarder ou même de stopper l’évolution de la maladie.
Ces deux articles importants font état de percées cruciales pour notre compréhension des bêta-amyloïdes et de notre capacité à traduire des données scientifiques fondamentales pour améliorer le diagnostic clinique et les stratégies thérapeutiques contre la maladie d’Alzheimer. Ces avancées nous donnent espoir qu’en dépit des derniers revers subis, de nouveaux traitements efficaces contre cette maladie dévastatrice pourraient être développés.
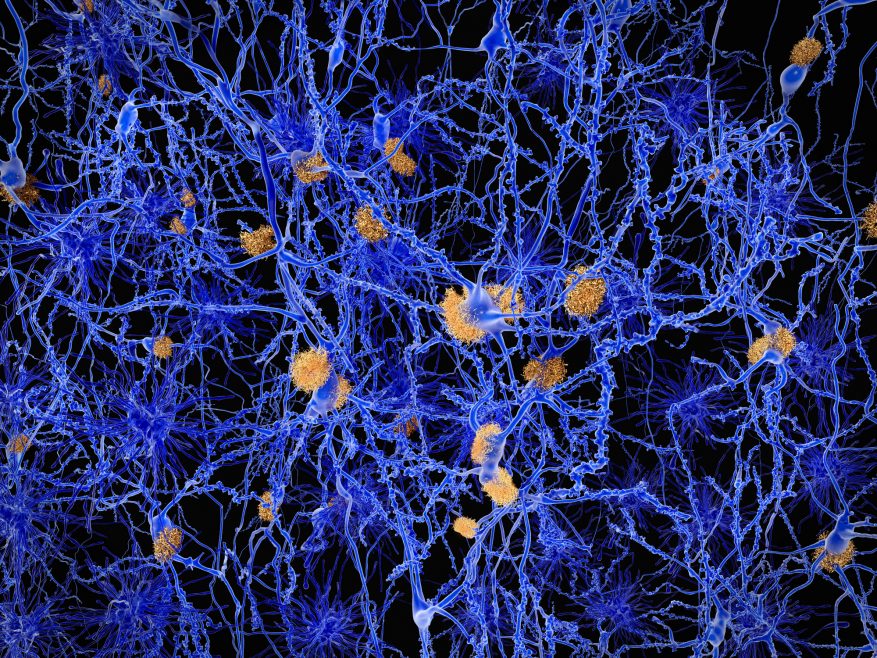
Image sélectionnée: Neurones avec plaques amyloïdes. Les plaques amyloïdes s’accumulent à l’extérieur des neurones et sont caractéristiques de la maladie d’Alzheimer. Ils conduisent à une dégénérescence des neurones affectés